Una molecola può cambiare il corso della Storia? A ben guardare: sì. La scoperta di come sintetizzare l’ammoniaca ha segnato un punto fondamentale di svolta nel mondo moderno ma la storia della sua scoperta e dei suoi primi utilizzi ci fanno riflettere. La drammatica storia di Haber, dell’invenzione delle armi chimiche e il triste destino che toccò alla sua famiglia e all’umanità a causa del suo operato
di Bianca Casale
// L’importanza dell’Azoto per la vita
L’ammoniaca, quella che troviamo sullo scaffale del supermercato nel reparto detergenti è un composto dell’azoto e come l’alcool etilico, la candeggina e l’acido muriatico è una sostanza di uso comune e nota da moltissimo tempo, fa parte integrante del nostro quotidiano.
La sua esistenza, a parte per economicità ed efficacia, passa inosservata.
Ma con un occhio un po’ più “chimico” l’ammoniaca (NH3) ha segnato un punto fondamentale di svolta nel mondo moderno ed è sicuramente stata una chiave di volta del Novecento.
La sintesi dell’ammoniaca a livello industriale è il motivo per cui sul nostro pianeta possono vivere più di sette miliardi di persone.
Ma noi non mangiamo certamente ammoniaca!
Giusta osservazione, ma alle piante invece l’azoto piace proprio tanto, è uno dei nutrienti più importanti (sotto forma di ione nitrato NO3– o di ione ammonio NH4+) tanto da trovarlo nella clorofilla e nelle proteine, in pratica viene coinvolto in tutte le fasi della vita di una pianta.
E nonostante l’azoto sia abbondantissimo (il 78% dell’aria che respiriamo) le piante non sono in grado di prenderlo e utilizzarlo direttamente. Devono per forza assorbire dal terreno, grazie alle radici, lo ione ammonio e lo ione nitrato.
La molecola di azoto è, infatti, una molecola estremamente stabile e non è facile convincerla a trasformarsi e legarsi con altri elementi. Non solo è un po’ snob, definiamola pure inerte.
L’ammoniaca e l’acido nitrico sono invece molecole che reagiscono molto volentieri. E indovinate quali sono i loro primi derivati? Proprio lo ione ammonio e lo ione nitrato.
E allora ecco che se vogliamo fare i conti con una crescita di popolazione ci tocca aumentare la resa dei campi e il letame e la rotazione annuale non basta più.
Abbiamo bisogno dei derivati dell’azoto.
Prima che ci accorgessimo dell’importanza dell’azoto come nutriente delle colture (lo scoprì Justus Von Liebig nel 1840), l’interesse per i composti dell’azoto era indirizzato quasi solamente al salnitro, che serviva per fare la guerra, per creare la polvere da sparo. Ma dopo che Von Liebig ci chiarì le idee, i concimi azotati per le colture divennero una sorta di ‘oro bianco’ e per questo le miniere da cui si estraeva il nitrato di sodio (nitro del Cile NaNO3) divennero estremamente importanti.
Così importanti da meritare una guerra a loro dedicata, la “Guerra del Pacifico” (1879-1884) tra Cile, Bolivia e Perù.
Ma ci accorgemmo in fretta che le miniere, data la crescente domanda di ‘oro bianco’ non sarebbero comunque mai state sufficienti.
Ed ecco perché la cruciale importanza della buona vecchia ammoniaca. Proprio da lei possiamo tirar fuori un sacco di preziosissimo ‘oro bianco’.
A primo acchito la molecola di ammoniaca sembra molto semplice, un atomo di azoto (N) e tre atomi di idrogeno (H) e dunque la reazione per crearla non dovrebbe costituire un problema. Peccato che azoto e idrogeno non abbiano moltissima voglia di mettersi assieme, ricordate l’azoto snob e inerte?
Come l’abbiamo risolta?
// La storia di Haber e le due facce della medaglia di una scoperta scientifica
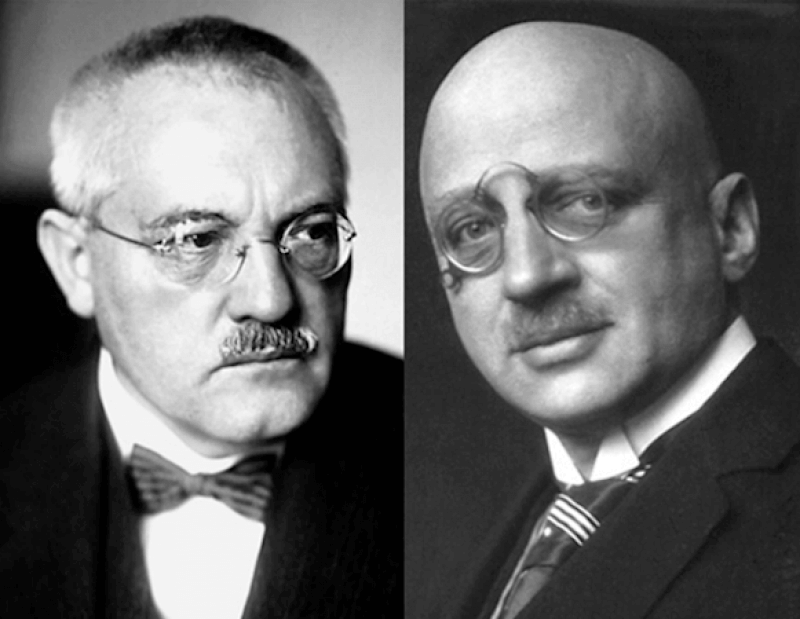
Tra il 1905 e il 1910 due chimici tedeschi, Fritz Haber e Carl Bosch, cambiarono tutto sviluppando il processo per la sintesi dell’ammoniaca a partire dagli elementi.
Fidatevi, la storia di questo processo merita d’esser letta, è il classico esempio delle possibili due facce della medaglia di una scoperta scientifica. La stessa scoperta può salvare l’umanità e cercare di distruggerla.
Fritz Haber nacque nel 1868 in Prussia da una ricca famiglia di origine ebraica specializzata nel commercio di prodotti farmaceutici e di pigmenti. Quindi nulla di strano se il giovane Haber mostra subito una propensione per la chimica. Fritz non mollò gli studi quando il padre sperava di passargli la gestione degli affari di famiglia andò a Berlino a proseguire la sua formazione sotto il tutoraggio di gente del calibro di Augustus Von Hofmann, considerato il padre della chimica organica. Haber si laureò con la lode e tornò in Prussia prima di trovare la sua strada come ricercatore al Politecnico Federale di Zurigo, successivamente a Jena, e infine, a Karlsruhe, dove restò per diciassette anni giungendo al titolo di professore ordinario.
Le sue ricerche sull’ammoniaca partirono sottotono e con risultati deludenti. Doveva lavorare ad altissima temperatura e la resa era troppo bassa. Così, abbandonò le ricerche ma le riprese quando iniziò una diatriba con Walther Nernst (altro luminare, stavolta in elettrochimica) e nel 1908 Haber riuscì a sintetizzare l’ammoniaca con condizioni e resa più accettabili grazie all’utilizzo di un catalizzatore a base di osmio.
Fu poi Bosch, che lavorava alla BASF ad ottimizzare il processo per gli usi industriali.
Per Haber fu l’inizio di una lunga carriera di successo. Prese il posto dirigenziale al nuovo istituto Kaiser Wilhelm per la chimica fisica e l’elettrochimica e collaborò con i maggiori esponenti accademici dell’epoca, compreso Albert Einstein. Siamo alle soglie dell’inizio del primo conflitto mondiale e durante la Prima guerra mondiale i nitrati furono strategici, non solo per l’uso come fertilizzanti ma anche per preparare le munizioni. La Gran Bretagna impose un blocco navale alla Germania che così venne tagliata fuori dalla fornitura di nitro del Cile e fu obbligata a utilizzare la nuova tecnologia di Haber-Bosch per sintetizzare l’ammoniaca e da esse i nitrati che tanto gli erano necessari.
Ma è qui che viene fuori il ‘lato oscuro’ della forza, Haber usò la sua influenza per convincere i gerarchi tedeschi che la guerra chimica avrebbe portato ad una  veloce risoluzione del conflitto diminuendo le vittime.
veloce risoluzione del conflitto diminuendo le vittime.
I gerarchi autorizzarono l’uso delle armi chimiche e fecero un test: nell’aprile del 1915 in Belgio, vicino a Ypres vennero rilasciate 167 tonnellate di cloro gassoso che portarono alla morte, tra atroci sofferenza, almeno mille persone. Il test fu ripetuto qualche giorno dopo, aggiungendo al macabro calcolo altri quattromila morti e diecimila feriti.
Al conteggio dei morti dobbiamo aggiungere anche la morte della moglie di Haber, Clara Immerwahr. Brava chimica anche lei e convinta pacifista, fu sconvolta dalle azioni del marito, le giudicava “una perversione delle scienza” e “un segno di barbarie, corrompere proprio la disciplina che mira a svelare i segreti della vita”.1
// Il suicidio della moglie, la disfatta della sua teoria sulle armi chimiche e la prosecuzione negli studi
Quando Haber ritornò da Ypres, promosso capitano, Clara si suicidò sparandosi proprio con la pistola del marito. Il figlio tredicenne Hermann la trovò in punto di

morte. Haber non si presentò nemmeno al suo funerale.
Imperterrito, proseguì la sua folle corsa e continuò a testare le armi chimiche e le ricerche in materia.
Purtroppo era molto bravo, e scoprì due molecole: il fosgene e l’iprite (da Ypres, conosciuta anche come gas mostarda) e decise anche di risposarsi nel 1917. Dopo il termine del conflitto, fu costretto a scappare in Svizzera per evitare il processo per la morte di 92mila soldati colpiti dalle armi chimiche di sua invenzione, i feriti furono oltre un milione – ma i numeri sono discordanti a seconda delle fonti, in alcuni casi i morti calcolati sono molti, molti di più.
La guerra non fu accorciata di un giorno, e le sue armi al posto di far uccidere meno persone come lui aveva affermato, furono invece una delle sorgenti della strage di persone della Prima guerra.
Penserete che sia finita qui, che Haber si sia ritirato a pensare ai suoi errori, invece no.
Tutto fu dimenticato e Haber tornò al lavoro e vinse addirittura il Nobel per le sue ricerche sulla sintesi dell’ammoniaca. Ovviamente la giustificazione non fu certo per l’impiego militare ma per il suo utilizzo per l’agricoltura.
Tornò al suo posto nell’istituto e segretamente continuò a studiare le armi chimiche con la benedizione del governo tedesco. Si interessò agli insetticidi e mise a punto il procedimento per la sintesi dell’acido cianidrico, denominato commercialmente Zyklon B, che teoricamente era destinato alla disinfestazione di pidocchi e che fu poi utilizzato per uccidere i prigionieri dei campi di sterminio nazisti.
Rimase al suo posto presso l’Istituto di Fisica e Elettrochimica della Società Kaiser Wilhelm di Berlino fino a quando, nel 1933 si vide costretto a lasciare il Reich in quanto di origine semita e oltretutto si oppose al licenziamento dei colleghi ebrei dell’istituto.
Morì l’anno successivo a Basilea e venne sepolto insieme alla povera prima moglie Clara.
Un dettaglio ulteriore: il figlio di Clara e Fritz, Hermann che aveva trovato la mamma in fin di vita, morì suicida nel 1946 negli States dove si era trasferito.
Ludwig (“Lutz”) Fritz Haber (1921-2004), figlio di Haber e di Charlotte sua seconda moglie, pubblicò un libro sulla storia del gas velenoso, The Poisonous Cloud.
Il male impersonato, da un lato.
Dall’altro il processo chimico che porta il suo nome ha dato la possibilità di produrre 180 milioni di tonnellate di ammoniaca per anno. L’88% di questi viene poi utilizzato per lo sviluppo di concimi. Il numero di esseri umani sulla terra nel 1900 era pari a 1,6 miliardi, oggi siamo oltre 7 miliardi e questo è stato possibile anche grazie allo sviluppo delle colture agricole fertilizzate con i concimi azotati economici e abbondanti.2
La Storia ci insegna a guardare tutti i punti di vista e giudicare in base ai fatti. In questo caso non è facile mettere sul piatto della bilancia l’operato di un uomo, sicuramente geniale, sicuramente egoista e certamente mosso da ragioni che la sua mente giustificava come positive.
La scienza non è buona o cattiva, l’uso che l’uomo ne fa può esserlo.
1 Goran Morris, The Story of Fritz Haber, University of Oklahoma Press (1967)
2 Giuseppe Alonci, Tutta questione di chimica, Giunti 2019
Spunti bibliografici:
Luigi Cerruti, Bella e potente. La chimica dagli inizi del Novecento ai giorni nostri, Editori Riuniti 2016








